
Prima è arrivato l’editing genomico classico, e per spiegare come funziona i ricercatori hanno usato la metafora delle forbici che tagliano il DNA. Poi è stato sviluppato il “base editing”, e lo hanno paragonato alla correzione manuale di un testo, fatta con gomma e matita. Ora che sulla scena si affaccia un altro approccio innovativo alla modificazione genetica, come possiamo descriverlo? “Immaginate un programma di videoscrittura al posto delle forbici e della matita”, ha detto David Liu presentando l’ultima tecnica messa a punto nel suo laboratorio al Broad Institute di Boston, durante la conferenza stampa organizzata da Nature.

Se l’ambizione ultima delle biotecnologie dell’era CRISPR è riuscire ad apportare qualunque cambiamento in qualsiasi punto del genoma, possiamo dire di esserci avvicinati all’obiettivo. La novità si chiama “prime editing” (la parola prime sta per avvio) ma è già stata soprannominata “editing trova-e-sostituisci” in omaggio alla funzione di word.
L’ingrediente chiave è lo stesso degli altri sistemi CRISPR, ovvero l’enzima Cas9, che ha il pregio di scorrere fino a posizionarsi nel punto prescelto del genoma. Assomiglia al cursore che lampeggia sullo schermo mentre scriviamo al computer, perché indica il punto in cui vanno a inserirsi le lettere. Nel prime editing, però, la Cas9 è doppiamente programmabile oltre che accessoriata con un nuovo dominio, per poter copiare alla lettera le istruzioni fornite dai ricercatori senza effettuare il classico taglio dei due filamenti e senza bisogno di fornire uno stampo aggiuntivo.
Per capire come funziona il meccanismo molecolare in dettaglio ci vuole un po’ di pazienza, ma ne vale la pena: il prime editing è così versatile che, in linea di principio, potrebbe correggere l’89% delle mutazioni che causano malattie genetiche nell’uomo.
Partiamo dunque dal modello più vecchio, la Cas9 che abbiamo imparato a conoscere nel 2012, con lo storico lavoro di Jennifer Doudna ed Emmanuelle Charpentier. Per trovare il sito bersaglio usa una molecola guida di RNA. Poi, una volta arrivata a destinazione, recide il DNA, consentendo ai ricercatori di inattivare il gene preso di mira. Il modello successivo, il base editing sviluppato da Liu a partire dal 2016, consente correzioni mirate a livello di singola lettera e si affida a un meccanismo leggermente diverso.
L’enzima Cas9 è ancora presente e resta programmabile attraverso la molecola guida, ma è stato privato delle forbici e fuso con un altro componente che converte chimicamente le lettere del DNA, cambiandone l’identità. Peccato che su 12 tipi di conversioni possibili, sia in grado di compierne soltanto quattro. Ad esempio non può trasformare la T (timina) in A (adenina), come sarebbe necessario per correggere l’anemia falciforme, e non può nemmeno operare piccole inserzioni o piccole delezioni mirate, come quella necessaria per rimuovere le quattro lettere extra nella malattia di Tay Sachs.

L’idea di progettare un nuovo modello capace di superare questi limiti è venuta al postdoc Andrew Anzalone, il primo firmatario del lavoro pubblicato su Nature insieme a Liu. Per prima cosa ha pensato di conferire un incarico aggiuntivo all’ RNA guida. “Ho immaginato che l’RNA potesse servire anche a portare le informazioni sui cambiamenti da effettuare”, ha spiegato Anzalone. Nel prime editing, dunque, si usa un RNA detto peg (prime editing guide) che non si limita a indicare il sito prescelto sul genoma, ma suggerisce anche quali refusi correggere. Per questo abbiamo detto che il sistema è doppiamente programmabile.
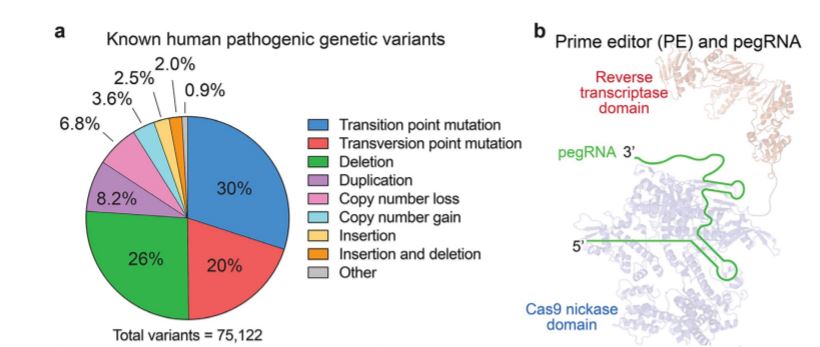
Quanto all’enzima Cas9, ha le forbici parzialmente disattivate come nel base editing, ma è fuso con un componente a cui finora non aveva pensato nessuno. Un enzima capace di trascrivere l’RNA in DNA, ovvero una trascrittasi inversa che legge il copione fornito dal pegRNA e lo ricopia lettera per lettera nel punto in cui si posiziona il cursore, senza bisogno di stampi aggiuntivi.
È probabile che in futuro ognuna delle tre vie all’editing troverà impieghi utili, perché ogni strumento ha i suoi punti forti e i suoi punti deboli. Ma i prime-editor sembrano destinati a primeggiare nelle applicazioni terapeutiche perché, come spiega Liu, “offrono una maggiore flessibilità nella scelta dei bersagli e maggiore precisione nell’editing”.
La parte del pegRNA che specifica la sequenza può essere progettata a piacimento, allo scopo di ottenere mutazioni puntiformi, delezioni su misura, inserzioni su misura e, volendo, tutte queste cose combinate insieme. Lavorando in vitro, Anzalone, Liu e colleghi hanno riparato le mutazioni dell’anemia falciforme e della Tay Sachs, raggiungendo rispettivamente un’efficienza del 55% e del 35% con pochissimi effetti indesiderati. Per testare la flessibilità del sistema, inoltre, hanno lavorato con 4 tipi di linee cellulari umane e hanno operato oltre 175 eventi di prime editing in cellule umane, tra cui 100 mutazioni puntiformi di tutti i tipi possibili, precise inserzioni lunghe fino a 44 lettere, delezioni precise lunghe fino a 80, e avrebbero potuto spingersi oltre.
A conti fatti i prime-editor non sbagliano quasi mai bersaglio e operano con una specificità sorprendente in corrispondenza del sito prescelto, grazie al particolare meccanismo di azione che prevede un maggior numero di appaiamenti con il DNA rispetto all’editing classico. In pratica l’upgrade ha fornito un sistema di sicurezza ridondante che offre più opportunità per bloccare il processo se qualcosa non torna.
Ora bisognerà lavorare per ottimizzare il prime editing per il maggior numero possibile di specie e linee cellulari, oltre a individuare i vettori più adatti per trasportare i prime-editor dentro le cellule (Liu e colleghi finora hanno usato con successo transfezione e lentivirus). Per essere soltanto il primo lavoro, comunque, è uno splendido inizio e Liu è fiducioso: “La comunità dell’editing è vibrante, penso che nei prossimi mesi centinaia se non migliaia di ricercatori proveranno a usare il prime editing contribuendo al suo sviluppo”.

Pingback: Prime, il nuovo editing genomico che reinventa CRISPR – Centro Studi Panzarella
Vorrei informazioni sui metodi usati,capire se si possono usare anche su altre alterazioni metaboliche. Se è possibile modificare un aminoacido sbagliato e aggiustare la catena.
"Mi piace""Mi piace"
l’articolo scientifico è appena uscito e lo trova linkato, comunque la mia risposta è che secondo gli autori il metodo potrebbe funzionare con quasi tutte le mutazioni che causano malattie genetiche (quando dicono 89% non contano le malattie causate da variazioni nel numero delle sequenze). Il punto è che siamo ancora in vitro, ovvero all’inizio della sperimentazione preclinica, la strada è ancora lunga.
"Mi piace"Piace a 1 persona