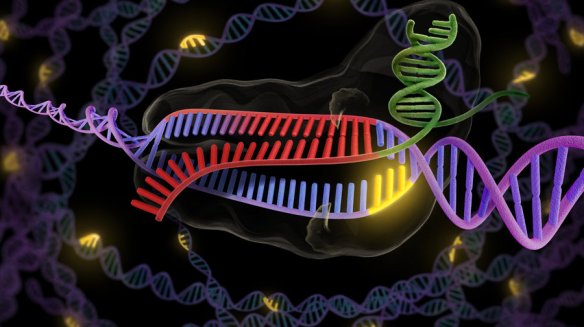
 Continua il viaggio nei laboratori italiani all’avanguardia nell’uso di CRISPR, la tecnologia emergente che sta rivoluzionando lo studio dei genomi. Dopo il CattaneoLab e l’Istituto Europeo di Oncologia, è la volta del laboratorio di uno dei pionieri del silenziamento dei geni. Pino Macino è uno dei ricercatori che hanno contribuito alla nascita di un settore di ricerca premiato con il Nobel nel 2006 (l’interferenza a RNA), insegna biologia cellulare alla Sapienza Università di Roma ed è convinto che CRISPR rappresenti un balzo in avanti straordinario per indagare la funzione dei geni e cercare di trasformare in farmaci le conoscenze sulle basi molecolari delle malattie.
Continua il viaggio nei laboratori italiani all’avanguardia nell’uso di CRISPR, la tecnologia emergente che sta rivoluzionando lo studio dei genomi. Dopo il CattaneoLab e l’Istituto Europeo di Oncologia, è la volta del laboratorio di uno dei pionieri del silenziamento dei geni. Pino Macino è uno dei ricercatori che hanno contribuito alla nascita di un settore di ricerca premiato con il Nobel nel 2006 (l’interferenza a RNA), insegna biologia cellulare alla Sapienza Università di Roma ed è convinto che CRISPR rappresenti un balzo in avanti straordinario per indagare la funzione dei geni e cercare di trasformare in farmaci le conoscenze sulle basi molecolari delle malattie.
 Lei è uno dei padri della vecchia tecnica che rischia di essere messa in ombra dalla nuova, perciò in un certo senso la sua opinione vale il doppio. Cos’ha di speciale CRISPR?
Lei è uno dei padri della vecchia tecnica che rischia di essere messa in ombra dalla nuova, perciò in un certo senso la sua opinione vale il doppio. Cos’ha di speciale CRISPR?
“Noi la usiamo per studiare la rete di relazioni dei micro-RNA, una famiglia di piccole molecole con importanti funzioni regolatorie. Per chi fa ricerca di base questa nuova tecnica è un’opportunità meravigliosa. Non renderà obsoleta l’interferenza a RNA, che continua a restare utile per alcuni studi, ma consentirà di rispondere a un’infinità di domande nuove”.
Quali sono le differenze fondamentali fra i due approcci?
Se si vuole studiare un gene il primo passo è silenziarlo, disattivando il gene stesso o il prodotto della sua espressione, e vedere cosa succede. L’interferenza funziona così: si introduce nelle cellule una molecola di RNA lunga 20-25 basi, complementare all’RNA messaggero derivato dalla trascrizione del gene. I due RNA si legano e questa molecola ibrida viene riconosciuta da un enzima capace di tagliare gli acidi nucleici, detto Argonauta. In questo modo il trascritto viene degradato e il gene è silenziato. Osservando cosa accade quando un gene non si esprime più si può indovinare la sua funzione.
Nella tecnica CRISPR non si usa Argonauta ma altre proteine che degradano il DNA in modo mirato, come la Cas9. Si ottengono risultati migliori?
Si agisce direttamente sulla sequenza del DNA anziché sull’RNA che costituisce il suo prodotto transitorio. Ad esempio si possono usare dei topi che esprimono la Cas9 in tutte le cellule, o solo in alcuni tessuti, e si possono introdurre mutazioni mirate nel genoma. In questo modo si può aggiustare un gene difettoso o mutagenizzare un gene ben funzionante e studiarne le conseguenze. Queste proprietà sono ereditabili. Insomma si ottiene una linea stabile di topi da usare come modelli delle malattie che affliggono la nostra specie. Un giorno verrà fatto anche sugli esseri umani, forse non solo a scopo terapeutico ma anche per potenziare caratteristiche che sono considerate positive. Ma è un futuro abbastanza lontano da pensare che io non lo vedrò e sono sollevato all’idea di non dover affrontare questi problemi etici.
CRISPR consente di giocare meglio e in modo duraturo con i livelli di espressione, quale applicazione considera particolarmente promettente?
Una possibilità entusiasmante è quella di usare delle proteine Cas modificate appositamente per continuare a sfruttare la loro capacità di riconoscere sequenze specifiche, ma senza tagliare il DNA. La Cas9 per esempio può essere legata a un altro enzima capace di modificare le proteine che avvolgono il DNA (gli istoni) per attivare o reprimere i geni di interesse. I farmaci che funzioneranno così saranno straordinari.
Le sequenze CRISPR, a cui la tecnica omonima si ispira, sono state scoperte confrontando delle sequenze batteriche depositate nei database. Biologia e informatica sono destinate a collaborare in modo sempre più stretto?
Alla Sapienza lo scorso anno abbiamo inaugurato una laurea triennale in bioinformatica per medicina, ingegneria e scienze, sono convinto che CRISPR renderà questo approccio sempre più utile e necessario. Ormai si possono costruire collezioni di cellule con mutazioni in tutti i geni, coprendo l’intero genoma. I biochimici non potranno più fare a meno di CRISPR e l’enorme mole di dati che verrà generata dovrà essere interpretata con la bioinformatica.
Per molto tempo il DNA ha oscurato l’RNA, nella ricerca e nell’immaginario. È ancora così?
L’RNA era considerato un oggetto, veniva usato e poi buttato via. Oggi è diventato un soggetto. Ci sono decine di migliaia di RNA che non codificano per proteine, ma fanno il mestiere dell’acido nucleico, assumendo forme tridimensionali che possono essere facilmente testate dall’evoluzione e che conosciamo ancora poco. Gli RNA interagiscono con il DNA, tra di loro e con le proteine, modificandone le proprietà. Mutagenizzando le regioni non codificanti del DNA, CRISPR aiuterà a decifrare anche questo complesso micro-mondo. Credo che faremo scoperte sorprendenti.
(Illustration courtesy of Jennifer Doudna/UC Berkeley)
